合成生物学结合了分子生物学、系统生物学和生物工程以全新的方式重新设计生物系统,让研究人员能够任意研究、改变、复制、甚至改造出复杂的生物路径、DNA基因序列与生物系统,进而为医学、制造业及农业等领域提供高效的解决方案。合成生物学一直是创新的引擎,不断推动我们对生物系统的重新构想。
泓迅科技自成立以来,一直致力于成为合成生物学领域的领军公司。我们依托完备的基因制造平台和生物设计平台,闭环满足DBTL技术需求,为合成生物学的发展和创新提供了强大的技术工具和解决方案。我们始终秉持科技创新的理念,持续提升服务能力和质量,透过深入的研究和前瞻性的专利,谱写这场生命的合成交响曲。
合成生物学核心策略—DBTL
合成生物学从底层脱氧核苷酸出发,经DNA小片段到DNA大片段乃至到整个基因组,从单一零散的元器件到功能模块再到整个生命系统网络,“自下而上”地逐级构筑生命活动,通过合成生物学的核心策略“设计?构建?测试?学习”(DBTL)来创造新功能生命体,实现从非生命物质到生命体系的跨越。
泓迅科技建立了先进的合成生物学赋能技术平台,提供完整的“设计—构建—测试—学习”各个环节一体化生物系统解决方案,为合成生物学应用领域的合作伙伴们提供序列设计、基因合成、基因编辑、文库构建、抗体工程、定向进化、蛋白表达、基因检测等多元化服务,满足不同阶段的研究需求。
泓迅科技DBTL的循环迭代过程:
设计(Design)阶段,借助计算机辅助设计,精心构建合成基因和生物回路。通过系统性的计划和模拟,能够在虚拟环境中预测生物系统的行为,为后续实验提供有力指导。
构建(Build)阶段,合成基因被引入生物体,开启合成生物学构建的关键步骤。这包括DNA的合成、大片段的组装以及基因编辑等技术手段。在这个阶段,理论的构想被具体地体现在生物体内,为测试和评估奠定基础。
测试(Test)阶段着眼于生物系统的性能评估。通过精密的实验和测量,能够获取生物体的实际行为数据。
最后,学习(Learn)阶段,根据测试结果进行深入分析,并结合学到的经验知识优化设计。通过迅速学习和调整,能够快速优化生物系统,不断改进设计方案,推动着合成生物学和生物制造的不断创新。
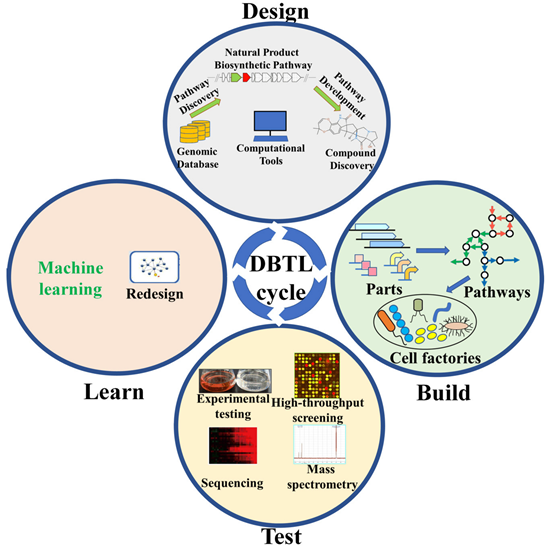
(Metabolites. 2021;11(11):785)
合成生物学构建专利—解锁创新之门
合成生物学构建了一个连接科学和创意的桥梁,打破了我们对生物学的传统认知。从微生物的工程到基因组合成,我们正在描绘一幅全新的DNA图谱,每一次合成都是对未知领域的探险,是对生命奥秘的深刻思考。我们骄傲地宣布,研究团队在合成生物学构建领域取得了里程碑式的突破,并成功获得了多项重要的专利,这些专利不仅仅代表了我们对科学的贡献,更是对合成生物学构建理念的印证。
(ZL201610670326 .4)
本发明提供一种重复性DNA的合成与组装方法,该方法包括重复性DNA序列分析;序列拆分与接口选择;引物的设计;DNA片段的合成;重复性DNA的组装。
专利亮点:
性能更加完善:增加了组装反应可靠性与稳定性,确保合成过程更为顺畅。
适用范围扩大:该方法可制备重复性DNA的PCR产物文库和重复性DNA的PCR产物,扩展了组装产物的适用范围。
(ZL202211134853 .5)
本发明通过CRISPR/Cas9方法对酿酒酵母基因组进行改造,获得了三种大片段DNA高效组装基因工程酵母菌Synbio?Sc1、Synbio?Sc2和Synbio?Sc3。
专利亮点:
可组装大片段DNA:基因工程酵母菌展现了卓越的能力,能够组装高达60kb的大片段DNA,为大片段DNA的组装提供了可行的解决方案。
高效率组装:组装效率高达63.5%至93.8%,这一技术突破有望在合成生物学与基因合成的工业研究与生产中发挥关键作用。
降低生产成本:本发明的基因工程酵母菌还具有降低生产成本的潜力,这为基因合成与合成生物学DNA构建的工业研究与生产带来了重要意义,为实现更经济高效的生物制造奠定了基础。
(ZL202210436102 .2)
本发明提供一种酵母细胞同源重组酶系与原核细胞表达重组酶的DNA体外组装试剂。
专利亮点:
全新构建方式:创新性地采用了DNA合成构建方式,首次提供了一种利用酵母细胞同源重组酶系以及部分原核细胞表达重组酶制备的DNA体外组装试剂。
高效快速组装:利用DNA体外组装试剂,可以对两端带有同源臂的DNA片段进行快速体外组装,实现单链与双链DNA的快速构建。该方法在仅1小时内单次可以完成4~40条单链引物或2~6个双链片段的无缝组装。
(ZL202211729510 .3)
本发明提供了一种基因突变文库的合成方法及其应用,所述方法包括:通过PCR反应将双链DNA转换成含有dUTP的单链DNA,通过梯度降温式退火反应将Trimer引物连接至上述含有dUTP的单链DNA上,退火后经过序列延伸、连接反应,形成Trimer结合下的双链杂合DNA突变序列集合,将所述集合经UDG酶消化后,进行PCR扩增,将扩增产物与载体重组连接形成重组质粒,即可得到基因突变文库。
专利亮点:
操作简单、综合成本低的PCR技术以及结合其它分子生物学技术,能够快速实现高正确率、高多样化的基因突变文库合成,尤其适用于一个在基因中的多个区域同时进行多样化文库构建。
提高了一个基因上多个可变区域同时多样化的效率,大大增加了突变序列的正确率,对抗体工程、酶工程、合成生物学等领域关键基因的挖掘与优化具有重要意义。
泓迅案例—复杂DNA合成组装
目的:合成组装14Kb的复杂基因片段,并将目的基因组装到pSynoYac0-Cm (约10Kb) 载体上。

难度分析:
目的片段中GC含量波动较大,局部区域甚至高达100%。
目的片段中有多个重复片段,直接重复649bp片段4个,1579bp片段2个,反向重复649bp片段4个,1299bp片段2个。

目的片段的GC含量分析图

目的片段的重复序列分析图
方法:
通过调整PCR反应体系中聚合酶、离子及其它组分含量,并优化退火温度、延伸时间等PCR扩增程序的参数,来保证PCR链式组装的成功率和保真性。
目的片段中有较多个超过500bp的重复序列,常规的组装方案很容易发生错配。针对这一难点,我们从开始就进行针对性设计及优化,灵活联用酶切连接、Golden Gate及Gibson组装等方法分段组装合成重复序列的中间构建。
结果:交付给客户的最终构建与客户需求的目的序列100%匹配。
泓迅案例—长DNA合成组装
目的:合成组装碱基长度为37848bp的目标片段,并将合成的片段组装至pSynoYac1-Cm (约10kb)上。

难度分析:
合成该目的片段需要400多条小片段寡核苷酸,进行80多次的重叠延伸PCR拼接组装,工作量较大,成功率较低。
序列的复杂度较高,GC含量波动大,长重复序列(≥20bp)多达108个。
38kb片段与10kb载体的组装难度大,成功率低。

目的片段的GC含量分析图

目的片段的重复序列分析图
方法:
用CRISPR基因编辑技术对酿酒酵母BY4741基因组进行了改造,开发得到一株酵母菌,显著提高了酵母体内同源重组的特异性、成功率以及组装稳定性。
针对片段缺失,改良酵母转化的操作流程和反应体系配方,显著增加了酿酒酵母大片段DNA的转化效率。
结果:通过上述一系列的优化改进,最终成功获得100%正确目的序列。
泓迅案例—基因突变文库合成
目的:对全合成人源化抗体序列的6个CDR序列区同时进行基因多样性变化设计,构建一种全合成人源化抗体基因突变文库。
难度分析:
目前市面上实现6个CDR序列区的每个氨基酸位点同时进行多样性变化的文库构建方法效率很低。
随着CDR区数目增多,每个CDR区的正确率无法保证。
方法:
通过PCR反应将全合成人源化抗体原DNA序列转换成含有dUTP的单链DNA;
通过梯度降温式退火反应将6个CDR区的Trimer引物同时连接至上述含有dUTP的单链DNA上;
步骤2退火后的序列经过延伸、连接反应,形成Trimer结合下的双链杂合DNA突变序列集合;
将上述集合经UDG酶消化,以消化产物为模板进行PCR扩增,获得目标基因特定区域多样化的突变序列集合;将所得序列集合与载体重组连接形成重组质粒,得到基因突变文库。

泓迅科技-创新型合成生物学赋能技术平台
泓迅科技以其先进的设计与制造为基础,致力于构建创新型合成生物学赋能技术平台。我们在基因合成、引物/探针合成、RNA合成、文库合成、重组抗体及蛋白表达、Sanger/二代测序、基因编辑等领域不断探索,将创新融入每一个环节,为客户提供高效、可靠的解决方案。
我们的团队拥有深厚的行业经验和跨学科背景,秉承着设计、构建、测试、学习(DBTL)的循环迭代原则,凭借独特的视角和前瞻性的思维,敢于挑战生物科技边界。
自成立以来,泓迅科技总计合成100亿碱基、100万修饰引物、100万基因。未来,我们还要合成更多产物。在无限合成的世界里,泓迅科技以创新为信仰,不断推动生物科技的进步,为构建未来的科技生态系统贡献力量。在这场掌握创新为主旋律的合成交响曲中,我们是开拓者,是引领者,是无限合成的创新者。无限合成,尽在掌握!
参考文献
[1] Wang J, Nielsen J, Liu Z. Synthetic Biology Advanced Natural Product Discovery. Metabolites. 2021 Nov 17;11(11):785.
| 免责声明:本文转载上述内容出于传递更多信息之目的,不代表本网的观点和立场,故本网对其真实性不负责,也不构成任何其他建议;本网站图片,文字之类版权申明,因为网站可以由注册用户自行上传图片或文字,本网站无法鉴别所上传图片或文字的知识版权,如果侵犯,请及时通知我们,本网站将在第一时间及时删除。 |